Actualité bibliographique de février
Revue d'études par Irène Gallais Sérézal, Julie Charles et François Aubin
Consensus Delphi des recommandations vaccinales pour les adultes avec psoriasis et rhumatisme psoriasique sous traitement systémique.
Chat VS, Ellebrecht CT, Kingston P, Bell S, Gondo G, Cordoro KM, Desai SR, Duffin KC, Feldman SR, Garg A, Gelfand JM, Gladman D, Green LJ, Gudjonsson J, Han G, Hawkes JE, Kircik L, Koo J, Langley R, Lebwohl M, Michael Lewitt G, Liao W, Martin G, Orbai AM, Reddy SM, Richardson V, Ritchlin CT, Schwartzman S, Siegel EL, Van Voorhees AS, Wallace EB, Weinberg JM, Winthrop KL, Yamauchi P, Armstrong AW. Vaccination Recommendations for Adults Receiving Biologics and Oral Therapies for Psoriasis and Psoriatic Arthritis: Delphi Consensus from the Medical Board of the National Psoriasis Foundation. J Am Acad Dermatol. 2024 Feb 6:S0190-9622(24)00243-3.
https://pubmed.ncbi.nlm.nih.gov/38331098/
Dans cette étude DELPHI (avis de 30 experts), les recommandations consistaient en :
- Aucune modification des traitements systémiques lors des vaccinations avec vaccins non-vivants
- Faire une pause de 2-3 demi vies avant la vaccination, et reprendre 2-4 semaines après.
Sécurité des combinaisons methotrexate et biothérapie dans le psoriasis modéré à sévère : une cohorte du registre BIOBADADERM
Lluch-Galcerá JJ, Carrascosa JM, González-Quesada A, Rivera-Díaz R, Sahuquillo-Torralba A, Llamas-Velasco M, Gómez-García FJ, Herrera-Acosta E, de la Cueva P, Baniandrés-Rodríguez O, Lopez-Estebaranz JL, Belinchón I, Ferrán M, Mateu A, Rodríguez L, Riera-Monroig J, Abalde-Pintos MT, Carretero G, García-Donoso C, Pujol-Marco C, Del Alcázar E, Santamaría-Domínguez C, Suárez-Pérez JA, Nieto-Benito LM, Ruiz-Genao DP, Salgado-Boquete L, Descalzo MÁ, García-Doval I. Safety of biologic therapy in combination with methotrexate in moderate to severe psoriasis: a cohort study from the BIOBADADERM registry. Br J Dermatol. 2024 Feb 16;190(3):355-363.
https://pubmed.ncbi.nlm.nih.gov/37846976/
Cette étude espagnole porte sur 2829 patients représentant 12853 patient-années. 1562 patients recevaient des anti-TNF, 238 des anti-TNF et du methotrexate, 1151 des anti IL-23, 114 des anti-IL23 et du methotrexate, 784 des anti IL-17, 89 des anti IL-17 avec methotrexate. Aucune augmentation des effets secondaires infectieux n’a été observée. Plus d’effets secondaires digestifs étaient observés dans l’associations anti-TNF et methotrexate. Au total ces données sont particulièrement rassurantes.
La dose cumulée de Methotrexate n’est pas associée à la fibrose hépatique chez les patients avec antécédent de psoriasis modéré à sévère.
Babakinejad P, Lapsley R, Forster L, McPherson S, Pearce MS, Reynolds NJ, Slack E, Weatherhead SC, Hampton PJ. Cumulative methotrexate dose is not associated with liver fibrosis in patients with a history of moderate to severe psoriasis. Br J Dermatol. 2024 Feb 17.
https://pubmed.ncbi.nlm.nih.gov/38366967/
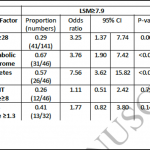
Cette étude anglaise porte sur 204 patients, recrutés entre juin 2020 et mars 2021. 91% avaient reçu du Methotrexate. La fibrose hépatique (LF) via le Liver stiffness measurement (LSM) était évaluée au fibroscanner. La LF était modérée si le LSM était >7,9kPA et sévère si >9,5kPa. La prévalence de le LF était de 25% and 17% pour le LF modérée et sévère respectivement. La dose cumulée de Methotrexate moyenne était de 2.16 g (IQR 0.93, 5.2) et n’était pas associée à la LF après ajustement sur l’âge le sexe, l’IMC, le score de consommation d’alcool, le syndrome métabolique et le tour de taille. La présence d’une obésité avec IMC>28, un syndrome métabolique, un diabète étaient de bons prédicteurs de l’élévation du score de fibrose au fibroscanner. Ces facteurs étaient supérieurs au FIB4 pour la prédiction de la fibrose hépatique dans cette cohorte.
Voir tableau 1
Effet anti-inflammatoire vasculaire des biothérapies chez les patients atteints de psoriasis : cohorte prospective basée sur TEP-scanner.
Boczar KE, Beanlands RS, Glassman SJ, Wang J, Zeng W, deKemp RA, Ward NC, Fehlmann CA, Wells GA, Karsh J, Dwivedi G. Anti-inflammatory effect of biologic therapy in patients with psoriatic disease: A prospective cohort FDG PET study. J Nucl Cardiol. 2023 Aug;30(4):1642-1652.
https://pubmed.ncbi.nlm.nih.gov/36754934/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10372102/
L’inflammation vasculaire chez les patients porteurs de pathologies inflammatoire chronique est un facteur de risque cardiovasculaire. Dans cette étude, 34 personnes ont été incluses, 11 traitées par biothérapie pour un psoriasis cutané ou cutanéo-articulaire (5 anti-TNF, 4 Anti IL-17, 2 anti IL12/23), 13 traitées par d’autres traitements (topiques ou photothérapie) et 10 contrôles sans psoriasis mais avec ostéoarthrite non inflammatoire. L’inflammation aortique était évaluée par le target-to-background ratio, TBR, sur la zone la plus inflammatoire, sur un TEP scanner à M0 et M6. Alors que les TBR étaient similaires à M0 entre les 3 groupes, seul le groupe traité par biothérapies présentait une baisse du TBR aortique à 6 mois de suivi. D’autres études avaient déjà montré l’effet anti-inflammatoire vasculaire sur des TEP scanner corrélé à l’efficacité des biothérapies. Reste à savoir si cette baisse s’associe à une réelle réduction du risque cardio-vasculaire dans cette population.
Voir figure 1
L’urticaire induit par l’ixekizumab est associée à une rémission courte du psoriasis, via l’activation des mastocytes.
Zhang L, Li X, Xu X, Le Y, Cao H, Zhang J, Xue F, Hu M, Xia Y, Pan M, Chen L, Zheng J. Ixekizumab-induced urticaria is associated with the short duration of remission in psoriasis by activation of mast cells. J Am Acad Dermatol. 2024 Jan 18:S0190-9622(24)00077-X.
https://pubmed.ncbi.nlm.nih.gov/38244613/
https://www.jaad.org/article/S0190-9622(24)00077-X/fulltext
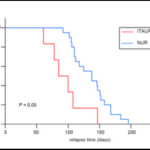
La dégranulation mastocytaire a été décrite dans la phase initiale du psoriasis, ainsi qu’au moment des rechutes. Sachant que l’urticaire complique 8% des injections d’ixekizumab, son association avec des rechutes précoces a été étudiée dans cette étude portant sur 26 patients. En plus des données cliniques, 6 patients avec urticaire induit par le traitement (ITAUR), et 8 patients sans (NUR) ont été analysés en histologie et analyse ARN. Le traitement était arrêté 24 à 32 semaines après avoir atteint un PASI 75. La présence d’une urticaire sous traitement ainsi que la présence de mastocytes IL-17+ dans la peau en rémission était associées à une récidive plus précoce à l’arrêt de cet anti-IL-17.
Voir figure 2